アルロースとは
天然でカロリーゼロの糖:アルロース
アルロース(英:Allulose)はブドウ糖や果糖と同じく、単糖(糖の最小単位)のひとつで、天然にはズイナという植物の葉に含まれています。ブドウ糖や果糖が1グラムあたり4キロカロリーのエネルギーがあるのに比べて、アルロースは0.39kcal/g(Metabolism. 2010;59(2):206-214)ですが、食品表示基準においては、エネルギー換算係数として0kcal/gが使用できます。甘さは砂糖の70%程度でスッキリして雑味もなく、<美味しい>糖質です。


日本(香川県)から始まったアルロースの販売は、現在では海外企業も参画して世界10カ国以上で行われています。アメリカや韓国などの国では栄養表示上「アルロースは糖類あるいは添加糖から除外できる」として、糖類摂取の制限がかからないものと判断しています。 砂糖の摂り過ぎが健康問題を引き起こしている状況を、砂糖の一部をアルロースに置き換えることで改善することができる「夢の糖」として注目されています。 アルロースはプシコース(英:Psicose)とも呼ばれ、両方が使われていましたが、2014年3月に開催した国際希少糖学会で、日本でも世界でもアルロースの呼称に統一することになりました。
日常の食生活にも微量に含まれるアルロース
希少糖は自然界での存在量が極めて少ないのですが、私たちが普段の食事で微量ながら食べています。下表は食品・メニューに含まれるアルロースの量を示していますが、普段の食事にもアルロースが含まれていることがわかります。しかし、その量はとても少なく、後に述べるような機能を得られるほどの量ではありません。
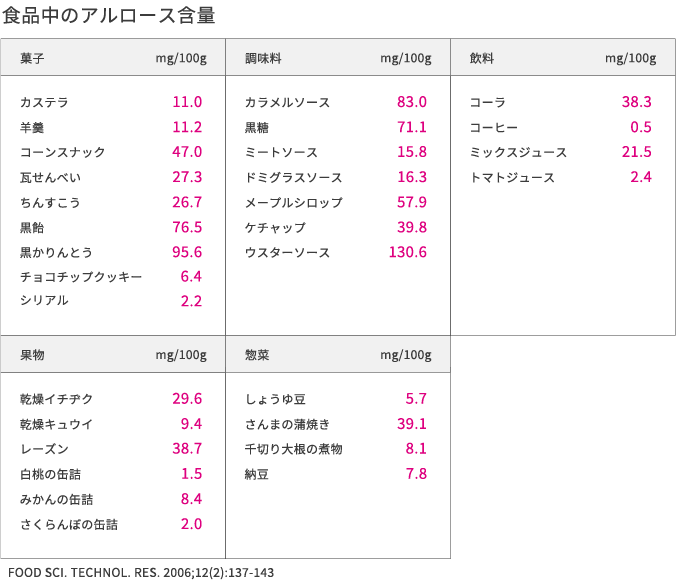
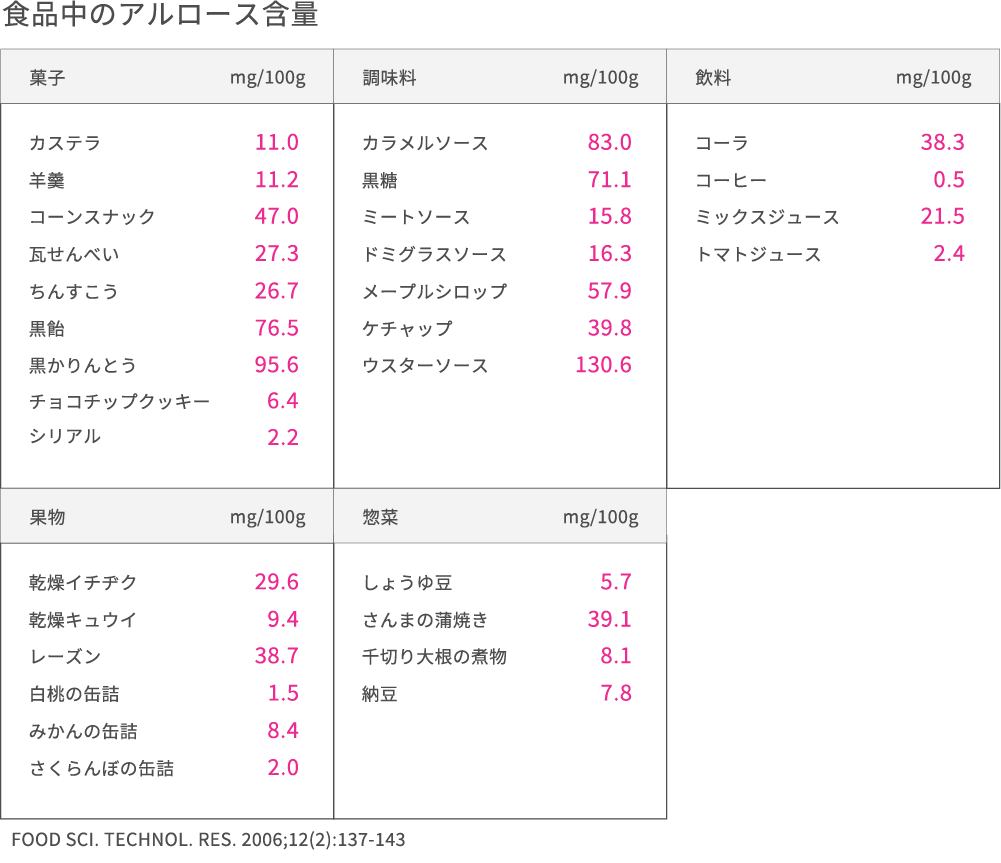
アルロースの化学式はブドウ糖や果糖と同じ!
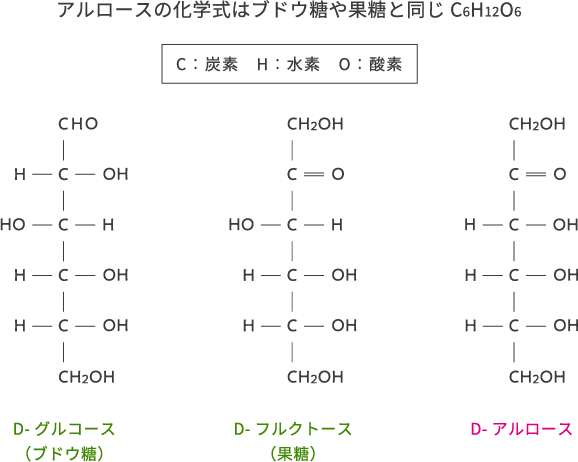
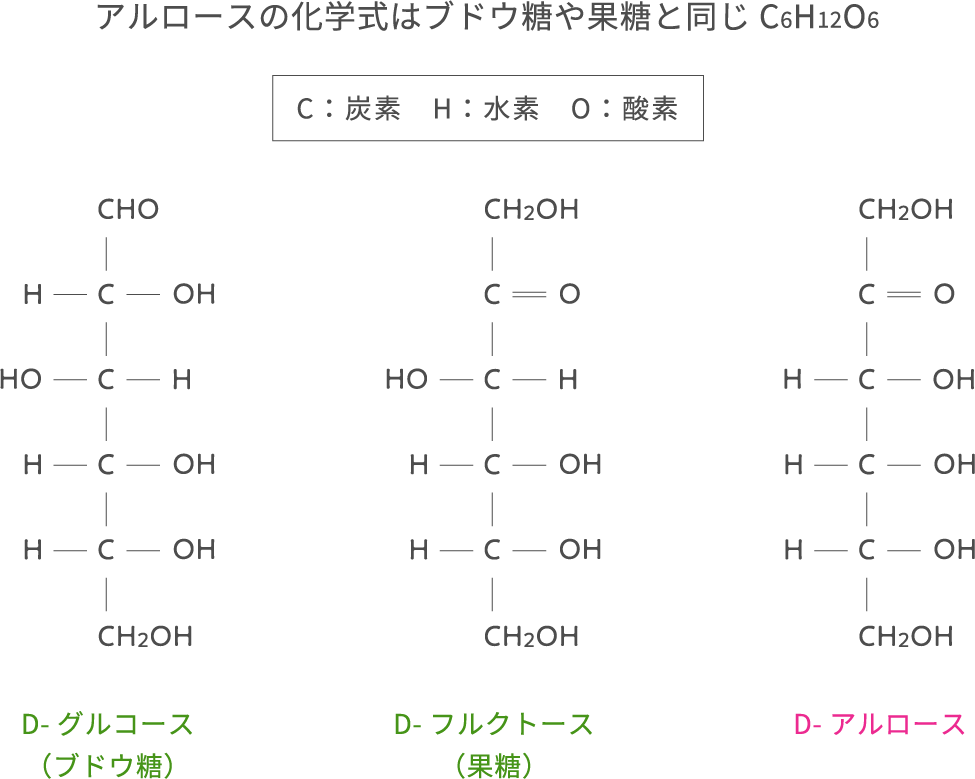
アルロースを化学式で書くとC6H12O6でグルコース(ブドウ糖)やフルクトース(果糖)と同じです。ただその構造は微細に異なっているため、性質や機能にも違いが生じます。図を見るとアルロースはグルコースよりもフルクトースによく似ていることがわかります。そのため物理化学的性質はフルクトースに似ています。
なお、アミノ酸や糖など、生命の素になる物質の分子の多くは「鏡像異性体」を持ちます。これは人間の右手と左手のような関係にあり、分子構造が対称なD型とL型が存在しています。自然界に豊富に存在する糖類の多くがD型であり、生産・研究が進み、事業化が始まっているのはD型のアルロース(D-アルロース)です。便宜上、D-を略して単にアルロースと呼びます。
アルロースに期待される健康機能
カロリーゼロであることに加え、アルロースにはさまざまな健康に良い機能性があることが研究によって明らかになりました。 それらの主なものは、食後血糖値上昇抑制作用と脂肪燃焼の促進作用です。これらの作用は生活習慣病である糖尿病や肥満(メタボリックシンドローム)の予防の可能性を示しています。また動物試験では運動やスポーツ時に用いることでその効果を高める働きも注目されています。 人生100年時代の到来に伴い、生活習慣病を予防し、また上手に付き合いながら、健康長寿を延伸することが求められています。以下にアルロースの持つ機能性について説明します。


血糖とは
血糖とは血液中のブドウ糖(グルコース)のことです。食事で炭水化物(デンプン)や砂糖を摂取すると、血糖値が上がります。これは動物が生きていくために必要な体の仕組みですが、ブドウ糖や果糖の摂取が多すぎると高血糖になり、糖尿病予備軍になる危険性を高めます。また、ブドウ糖の余剰分は 腸で吸収された後に脂肪に変わり、蓄積されて肥満につながります。生活習慣病の予防には、適正な血糖値を保つことが大切なのです。
アルロースによる食後血糖値上昇抑制のメカニズム
アルロースには、食後血糖値の上昇を抑制する複数の作用点があることが、香川大学をはじめとする研究機関で明らかにされました。
糖の消化吸収の仕組みは以下のとおりです。デンプンはブドウ糖が数百個つながったもので、砂糖はブドウ糖と果糖とが1個ずつ結合したものです。これらを食事として摂取すると、消化管を通過する間に各種消化酵素により消化を受けて、最終的にブドウ糖や果糖にまで分解します。ブドウ糖や果糖は小腸の腸内壁にある単糖を取り込むゲート(トランスポーター)を通って吸収され、腸に豊富に分布している毛細血管に運ばれます。消化酵素による分解が単糖まで進んでいなければ小腸から吸収されることはありません。
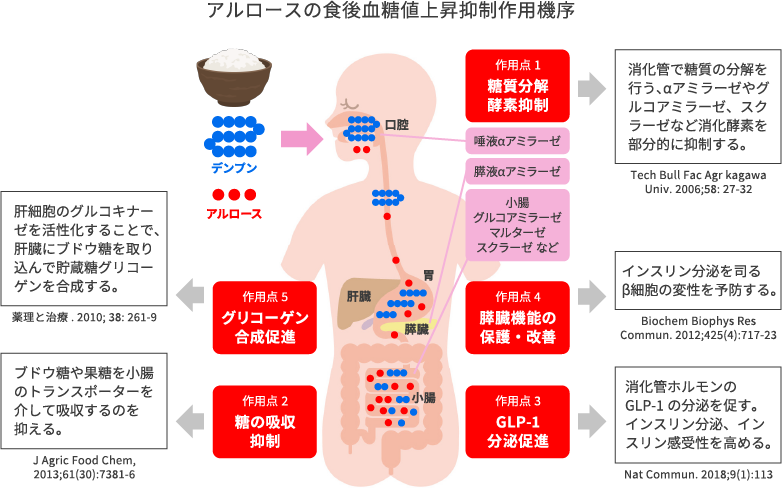
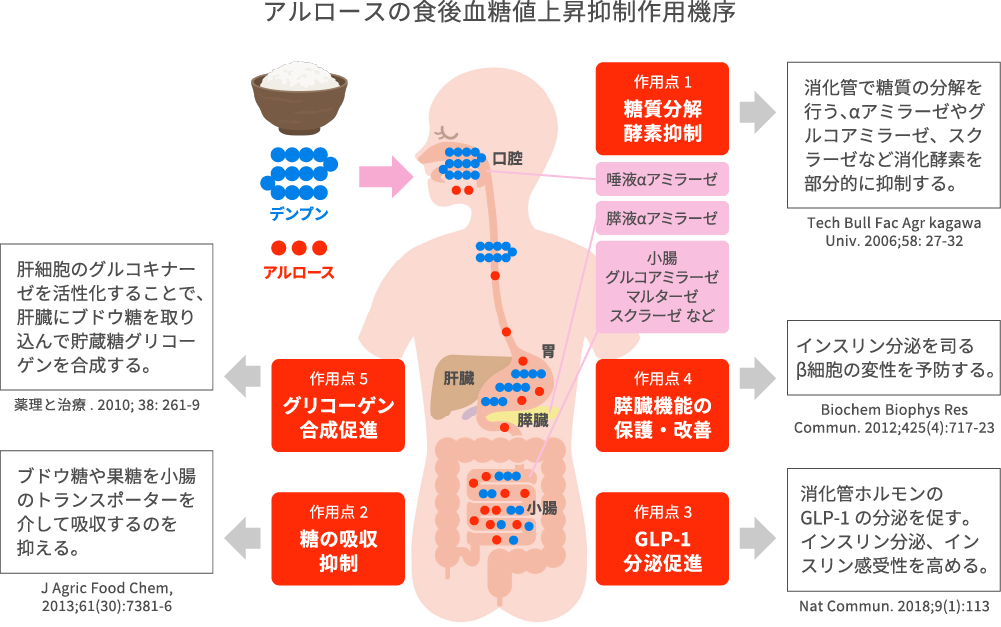
アルロースは消化酵素の働きを抑制する作用を持っています(作用点1:Tech Bull Fac Agr Kagawa Univ. 2006;58: 27-32)。そのため、デンプンや砂糖の消化速度が遅くなり、ブドウ糖や果糖にまで分解される量が少なくなるため、小腸から吸収される量が減るわけです。 次に、小腸でのブドウ糖や果糖の吸収を抑制する作用です(作用点2;J Agric Food Chem, 2013;61(30):7381-6)。アルロースはブドウ糖や果糖と同じC6H12O6の化学式をもつ単糖で、トランスポーターを通過します。ブドウ糖や果糖とともにアルロースが存在すると、トランスポーターの部分で競合が起こり、ブドウ糖や果糖の通過がアルロースにより邪魔されてしまいます。このためブドウ糖や果糖の血中への移行も減ります。
以上のような仕組みによって、アルロースは小腸でブドウ糖や果糖の吸収を阻害し、血糖値の上昇を抑えることができるのです。
さらにアルロースには、小腸のL細胞という細胞から分泌されるホルモンであるGLP-1(Glucagon-like Peptide 1)の分泌を促す働きがあることが発見され、大きな反響がありました(作用点3;Nat Commun. 2018;9(1):113)。GLP-1は血糖値を下げるホルモンであるインスリンの分泌を促し、インスリンが効きにくい状態(インスリン抵抗性)を改善するなどの働きがあります。GLP-1と同様の働きを持つ化学物質(GLP-1受容体作動薬)が合成され糖尿病治療薬として用いられていますが、アルロースはこのような化合物と異なり、本来我々生体が持つGLP-1の分泌を緩やかに促進する「GLP-1リリーサー(放出物質)」として働くのです。GLP-1の分泌促進を介した血糖値上昇抑制作用が起こります。
そのほかにも、膵臓においては、血糖値を下げるホルモンであるインスリンを分泌するβ細胞の保護作用が示されました(作用点4;Biochem Biophys Res Commun. 2012;425(4):717-23)。血糖値が高い状態では、β細胞はインスリンを分泌して血糖値を下げようとしますが、これが長く続くとβ細胞は次第に機能不全を起こしインスリン分泌が悪くなり、ついには変性して死んでしまいます。アルロースを投与していることでβ細胞をこうした変性から保護する作用が見つかっています。この作用は特に糖尿病病態において期待できます。
アルロースは肝臓においては、肝細胞のグルコキナーゼの核外移行を活性化することでグリコーゲン合成を促進し血糖値を下げます(作用点5;薬理と治療. 2010; 38: 261-9)。グルコキナーゼは血糖値が低い時にはグルコキナーゼ活性調節たんぱく質と結合して肝細胞の核内に存在していますが、血糖値が上昇し肝細胞内へのグルコース取り込みが増えると、活性調節たんぱく質との結合が解かれ細胞質に移行して、グルコースをリン酸化してグルコース-6リン酸を生成しグリコーゲン合成が進みます。アルロースはこの過程を促進して、血中からより多くのグルコースが肝細胞へ取り込まれることで血糖値を下げます。
このように、アルロースは複数のメカニズムを介して食後の血糖値上昇を抑え、高血糖状態を起こりにくくします。高血糖状態で使われずに余った糖は脂肪に変えられて体内に蓄積するので、その蓄積量を減らすことにもつながります。
ヒト試験でのアルロースの食後血糖値の上昇抑制効果
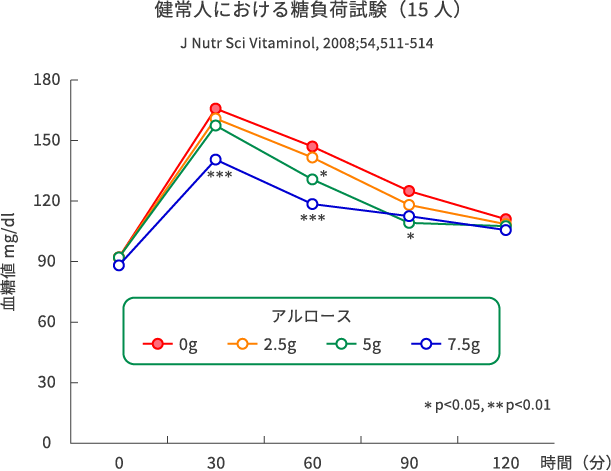
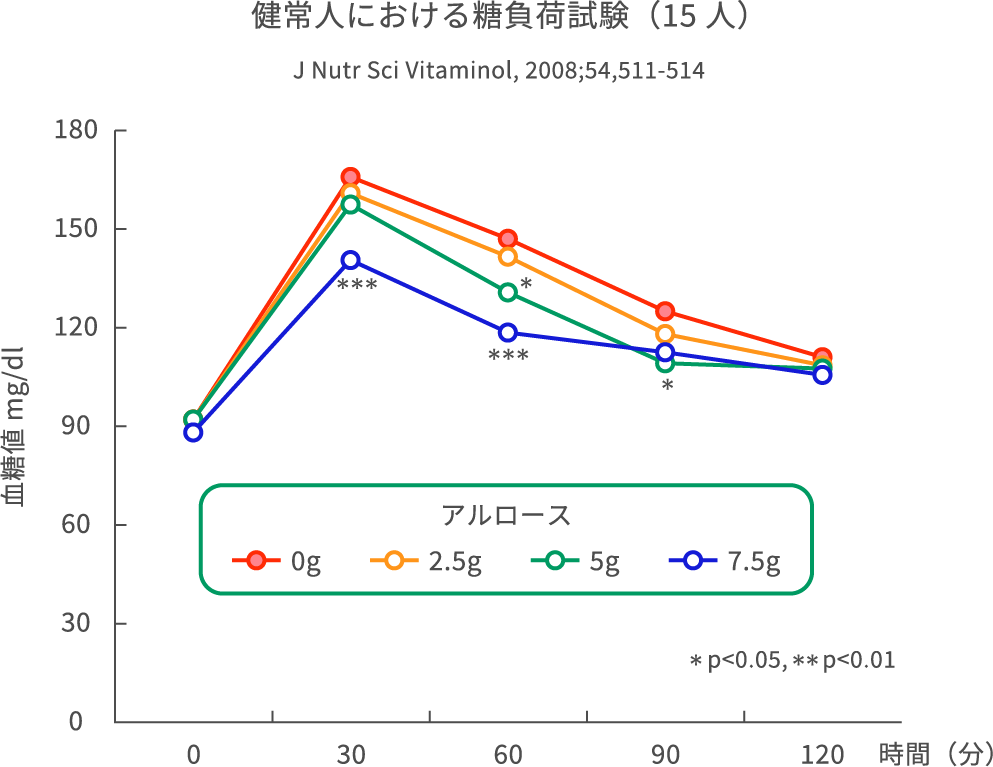
ヒトでの試験で、アルロースの食後血糖値上昇抑制作用を調べました。臨床検査でよく用いられる75g経口糖負荷試験を、健常人15名に行ったものです。被検者は空腹状態で75gのデンプン部分加水分解物液の入った飲料を与えられます。その際にアルロース0g、2.5g、5.0g、7.5gを一緒に飲んでもらいます。飲む直前と、飲んでから30分、60分、90分、120分時点の計5回採血を行い、血糖値を測定し血糖曲線を描きます。アルロースの量が増えるにつれて、血糖曲線が下がっている(赤⇒オレンジ⇒緑⇒青)のがわかります(J Nutr Sci Vitaminol, 2008, 54, 511-4より作成)。特に5.0gと7.5gでは、統計学的に有意差をもって血糖値の低下が認められました。
また次に2型糖尿病境界領域*の被験者15名に対して食事負荷試験を実施しました。健常人で効果の認められたアルロース5gを加えた飲料を食事と共に摂取した被験者は、プラセボ群(アスパルテーム10mg)と比べて、食後血糖値の上昇を抑えられることが示されました。糖尿病予備軍の方にも有効であることが示されました。(Biosci. Biotechnol. Biochem. 2010, 74, 510-9より作成)
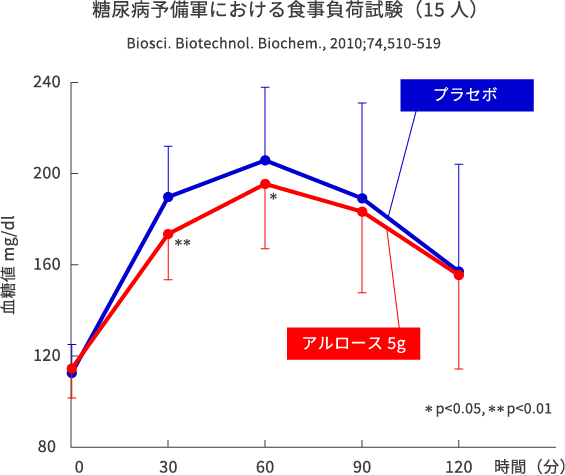
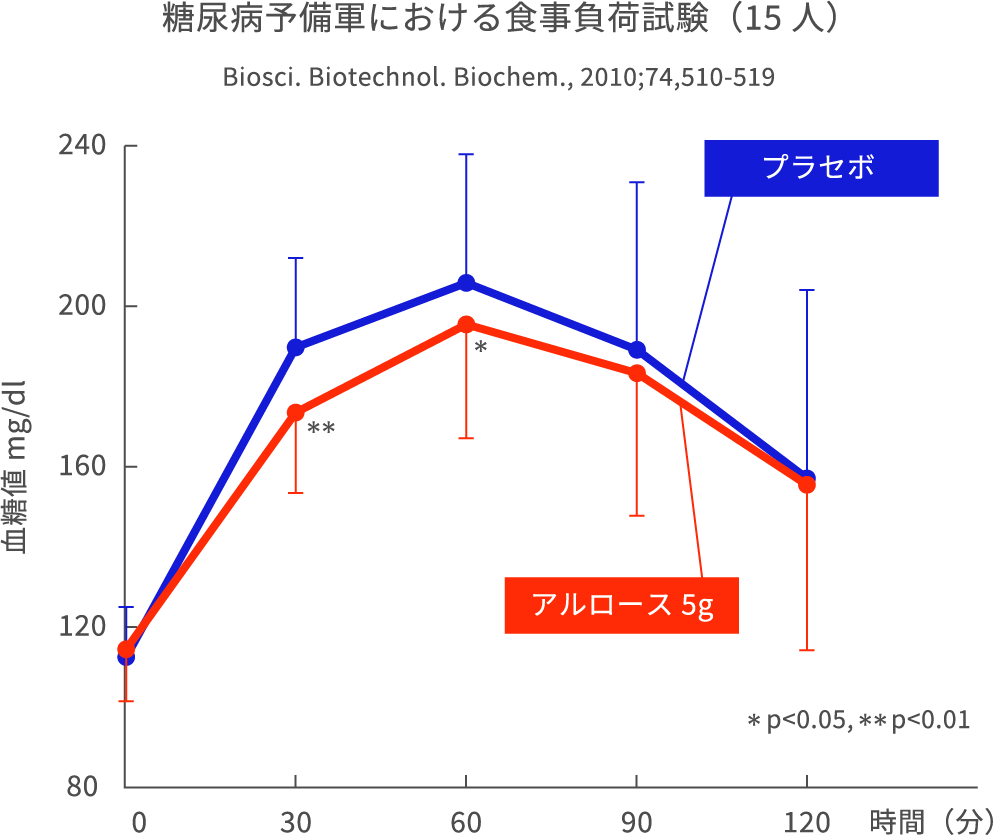
2型糖尿病とは、食事や運動などの生活習慣が関係して発症し、インスリン分泌低下・インスリン抵抗性(働きが悪い状態)が成因となるものです。高血糖であっても、糖尿病と診断される値と正常血糖値との間に血糖値が位置する場合を境界領域としています。一般的に、この領域に当てはまる人は糖尿病予備軍として捉えられます。
香川大学では、2型糖尿病患者に対するアルロースを含む糖尿病食の有効性を検討しました。標準的な糖尿病食と毎食8.5 gのアルロースを含む糖尿病食を摂取した後のピーク食後血糖値(PPG)を比較したところ、アルロースを含む糖尿病食は、標準糖尿病食と比較して、2型糖尿病患者のPPG値を改善しました。そして血糖値低下によるインスリン必要量の減少により、内因性膵臓インスリン分泌能力に対する保護効果も示しました(Nutrients. 2023;15(12):2802)。同グループはアルロースを用いた新たな糖尿病治療食の開発に踏み出しています。
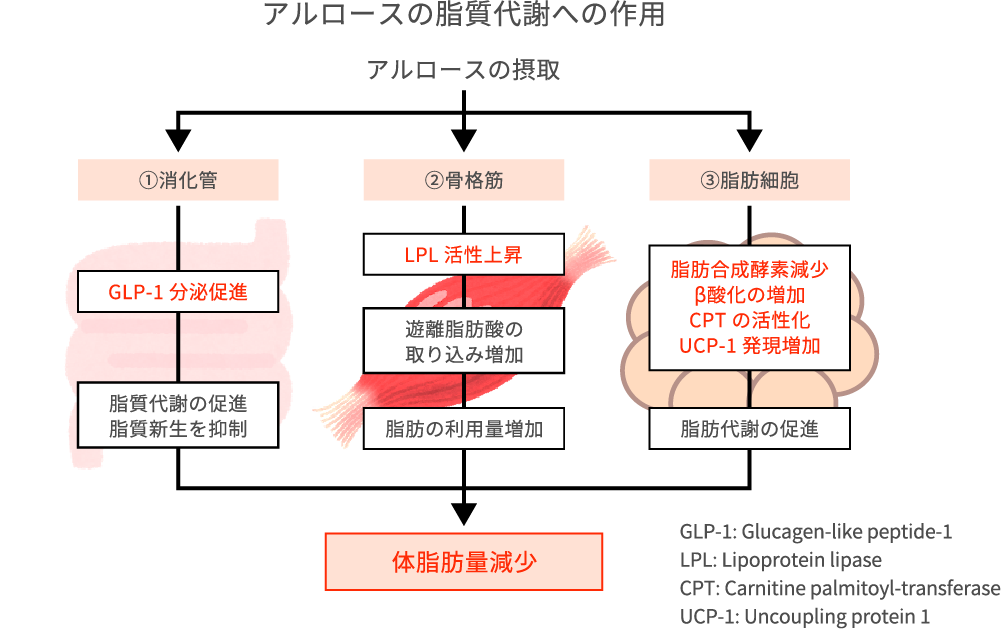
アルロースには、脂質代謝を亢進する機能があることが分かってきました。アルロースのいくつかの作用が報告されています。
第一に、血糖上昇抑制作用で説明した消化管ホルモンのGLP-1を介したものです。GLP-1には脂質代謝を高める働きがあり、余分なエネルギーを脂肪として蓄えている白色脂肪細胞を、余分なエネルギーを熱にかえて放出する褐色脂肪細胞に変えます。最近ではGLP-1受容体作動薬は抗肥満薬としても注目されています。
第二に、アルロースは、骨格筋では血液中から筋肉細胞への遊離脂肪酸の取り込みを増やして脂肪の利用を増やします。
第三に、脂肪細胞において脂肪の燃焼を促進します。脂肪細胞のミトコンドリアにあり脂肪の燃焼を促すUCP-1(Uncoupling Protein 1)の発現を高めます。
これらの作用により、身体全体の脂質燃焼効果を高めています。

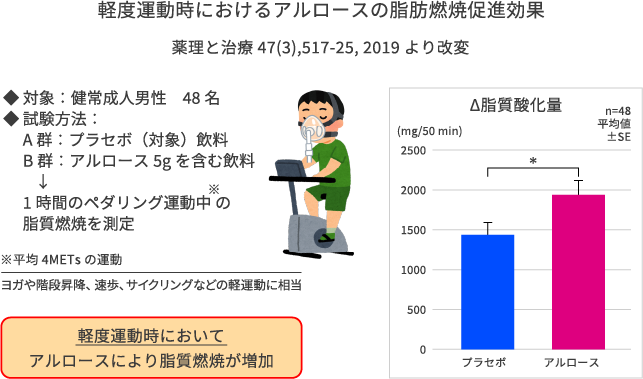
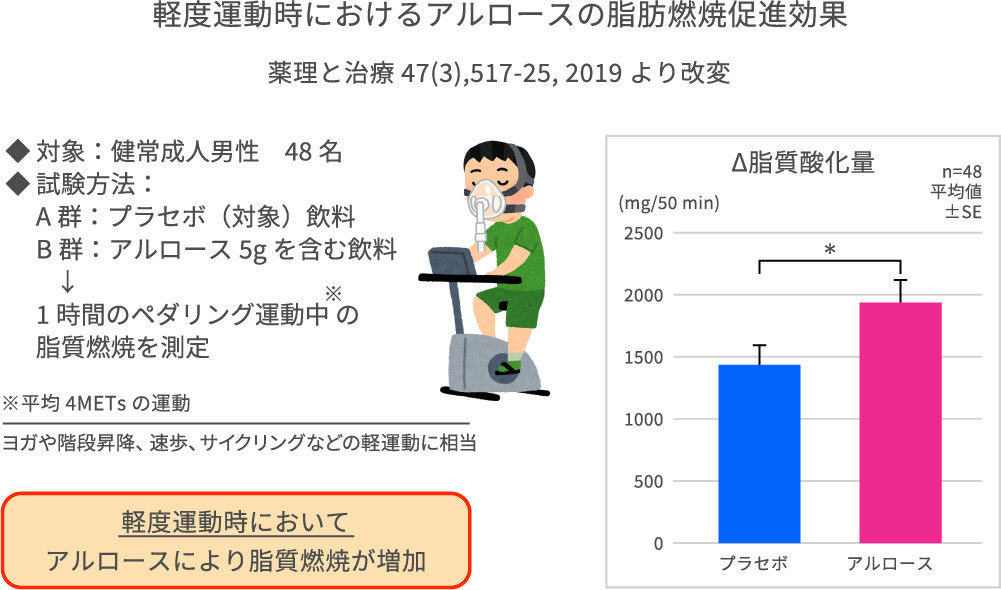
ヒト試験でもアルロースが脂肪の燃焼を促進することが示されました。 健常成人男性48名を、アルロース5gを含む飲料を飲んだ群と、含まない飲料(プラセボ)を飲んだ群に分け、1時間の軽度運動(ペダリング)をしてもらいます。吐く息を全て回収して分析することで体内で燃焼した脂肪の量を測定することができます。
この結果、アルロースを含む飲料を飲んで運動をすることで脂肪の燃焼が3割程度増加することがわかりました(薬理と治療. 2019; 47(3); 517-525)。また驚くことに、同様の研究を非運動時(臥位や座位で4時間過ごす)においても実施しましたが、アルロース5gを飲むことにより脂肪の燃焼が高まることが示されました。
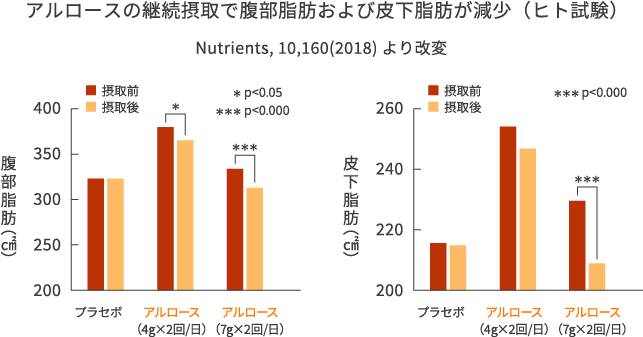
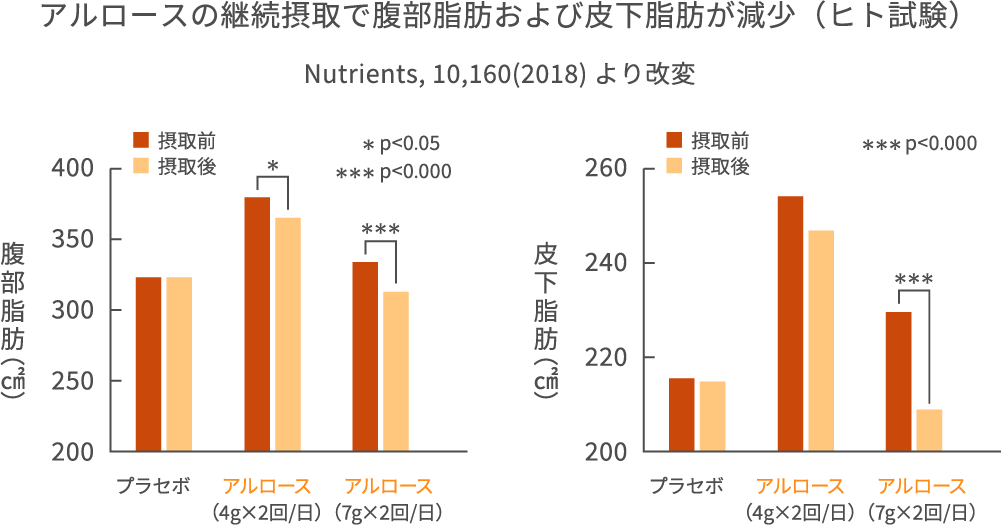
また、121人の軽度肥満の被験者(20~40歳、BMI 23 kg/㎡)を対象にアルロースの長期投与試験が行われました(Nutrients. 2018:10, 160)。被験者をプラセボ群(スクラロース12mg)、アルロース低用量群(4g)、アルロース高用量群(7g)の3群に分け、1日2回、12週間にわたりスクラロースあるいはアルロースを摂取しました。
その結果、アルロースは腹部脂肪と皮下脂肪を減少させることが示されました。
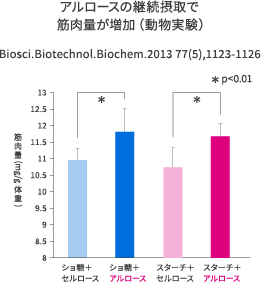
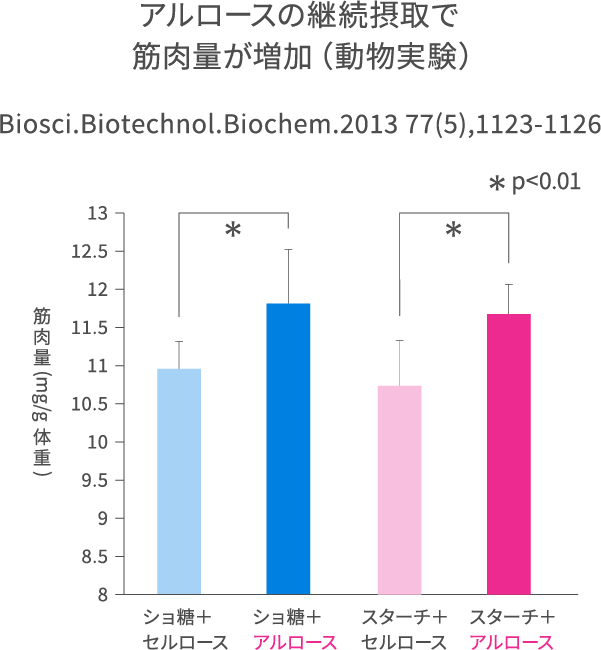
アルロースと運動やスポーツの効果が注目されています。動物実験の結果ですが、アルロースを継続摂取することで筋肉量が増えたり、運動後の疲労回復を早めたり、持続力が高まることが分かりました。今後ヒトでの検討が必要ではありますが、新しいアルロースの展開を期待させるものです。
高ショ糖食あるいは高コーンスターチ食の2種類の飼料において、それぞれアルロースを5%添加したものと、比較のため5%セルロースを添加した飼料を作り、16週令のWistarラットを4群で8週間飼育しました。飼育終了後、筋肉量を比較したところ、図で示すようにどちらの飼料でも、アルロースを添加した飼料で飼育した群で、筋肉量が約10%程度多かったのです。この時の体重はアルロース群の方がセルロース群に比べて減少しているのです。アルロースの摂取で体重は減るにもかかわらず、筋肉量は増えるという結果で注目されます(Biosci. Biotechnol. Biochem. 2013;77(5):1123-1126)。
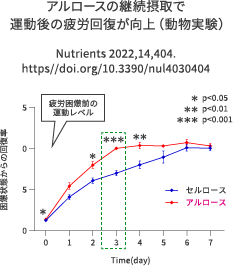
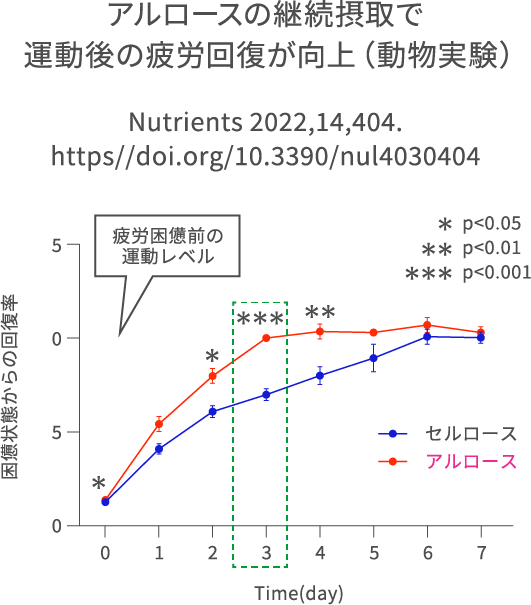
マウスを用いた実験では、4週間にわたって3%のアルロースあるいは3%セルロースを含む飼料でホイールケージを用いて飼育しました。飼育終了前にトレッドミルを用いた有酸素運動をさせたところ、マウスの走行距離が延びるとともに、運動後の疲労回復力が高められました(Nutrients. 2022;14,404. https//doi.org/10.3390/nul4030404)。 疲労困憊するまでトレッドミル運動をさせたマウスが元の自発運動量まで戻るまでの期間を測定したところ、セルロース添加飼料で飼育したマウスが6日間かかったところ、アルロース添加飼料で飼育したマウスでは3日間で回復しました。
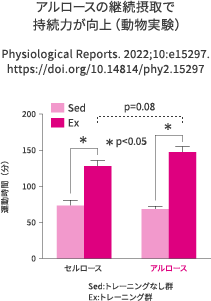
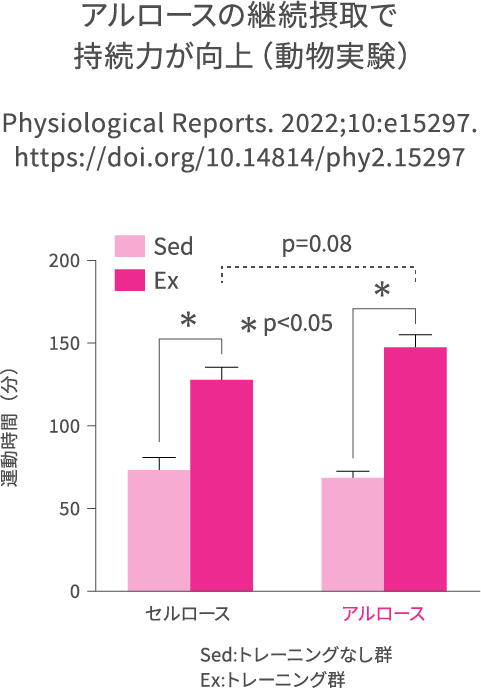
同じく、アルロース添加飼料とセルロース添加飼料で飼育したマウスにおいて、週5日のトレッドミルを用いたトレーニングにより持続力が向上するかどうかを調べたところ、どちらの飼料で飼育してもトレーニングした群はトレーニングをしていない群よりも大きく持続力がアップしましたが、アルロース群でより運動時間が延長しました(Physiological Reports. 2022;10:e15297. https://doi.org/10.14814/phy2.15297)。 いずれも動物実験での効果ですので、今後ヒトでの検証をする必要がありますが、大いに期待感を抱かせてくれる結果です。
食事や運動などの生活習慣が乱れていると、様々な生活習慣病が起こりやすくなります。肥満に始まり、高血圧、糖尿病、脂質異常症(高脂血症)などの生活習慣病が起こりやすくなります。そして、これらの生活習慣病は、さらに狭心症や心筋梗塞などの虚血性心臓病や脳卒中などを引き起こす下地となります。生活習慣の乱れからまるでドミノ倒しのように次々と悪影響が広がってしまいます。 特に注意すべき生活習慣病は、高血圧、糖尿病、脂質異常症です。これらは遺伝的素因も関係していますが、毎日の食習慣などの生活習慣が深く関係しています。そのため、日頃の生活習慣を見直し、高血圧、糖尿病、脂質異常症に至る前に問題点を是正することが大切です。
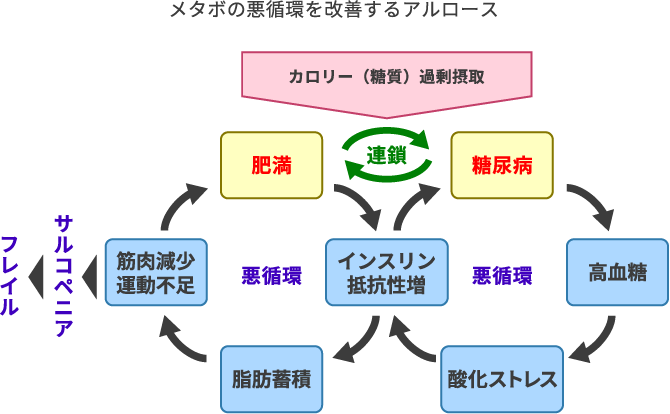
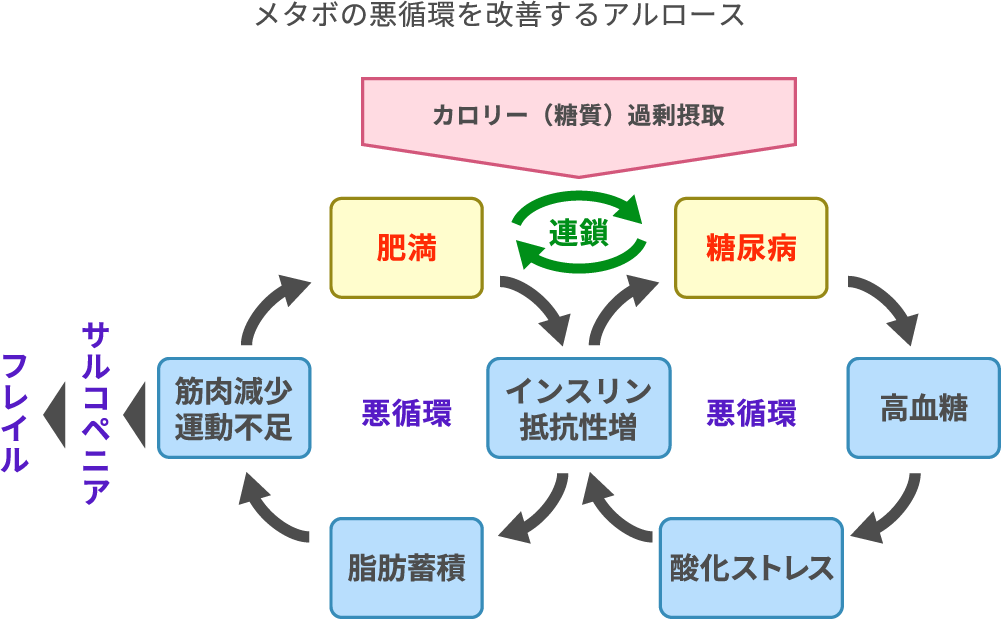
糖尿病による高血糖状態が長く続くと、酸化ストレスが高まるとともに、糖とたんぱく質とが結合してできる最終糖化産物(AGEs:老化物質とも呼ばれ、糖尿病や動脈硬化やアルツハイマー病などの悪化に関与します)が体内で多く作られます。さらに膵臓で作られて血糖値を下げるホルモンのインスリンが効きにくくなる状態(インスリン抵抗性)を生じるため、インスリンが作られていても血糖値がなかなか下がらないという悪循環が生じます。 またインスリン抵抗性が高まると体内への脂肪蓄積が増えます。この状態が筋肉減少を引き起こし、肥満による体重増加と相まって運動不足が生じることが、さらに肥満を悪化するという悪循環が生じます。筋肉減少(サルコペニア)は、さらにフレイル(心身の衰弱)を引き起こすリスクを高めます。糖尿病と肥満の悪循環は相互の連鎖を起こすため、厄介なのです。
アルロースはカロリーゼロの糖質としてカロリー摂取量を抑えることができるだけでなく、血糖上昇を抑えて高血糖状態を軽減し、酸化ストレスを減らします(Int J Vitam Nutr Res. 2020;90(3-4):210-220)。インスリン抵抗性が改善されて糖尿病の改善が期待できます。アルロースそのものの脂肪燃焼促進作用に加えて、インスリン抵抗性を改善することで、脂肪の蓄積量が減り、筋肉量の減少も防ぐことができます。このように糖尿病や肥満の悪循環を改善するように働くことが期待できるのです。日本人をはじめとする東洋人では、糖尿病により肥満が助長され、肥満により糖尿病も悪化するという連鎖が起こりやすいので、アルロースによりこの連鎖を断つことも重要です。サルコペニアを予防し、身体や心のフレイル(虚弱)状態を予防するということも期待できそうです。
アルロースは、 SDGs の観点からも注目されています。「SDGs」(持続可能な開発目標)は、2015年9月の国連サミットにおいて採択された「持続可能な開発のための2030アジェンダ」に記載された国際目標です。「地球上の誰一人取り残さない」ことを理念とし、人類、地球およびそれらの繁栄のために設定された行動計画であり、17のゴールと169のターゲットで構成されています。


SDGsの目標3は、「あらゆる年齢のすべての人々の健康的な生活を確保し、福祉を促進する」のテーマのもと、13個のターゲットから構成されています。そのうちの3.4と3.dが強く関連します。 ターゲット3.4は、「2030年までに、非感染症疾患(NCD :Non-communicable diseases)による早期死亡を、予防や治療を通じて3分の1減少させ、精神保健および福祉を促進する」です。NCDは生活習慣病と同義語です。
ターゲット3.dは「すべての国々、特に開発途上国の国家・世界規模な健康リスクの早期警告、リスク緩和およびリスク管理のための能力を強化する」です。 アルロースの普及により、糖尿病や肥満の生活習慣病(NCD)の予防や改善を実現し、早期死亡を減らすことにつながります。それを開発途上の国を含めて世界規模で展開しリスク緩和やリスク管理能力を強化することを目指します。
アルロース製品の使用にあたり
アルロースは希少糖のひとつであり、もともと自然界にも存在しています。従って自然界への負荷も少ないと考えられます。アルロースには毒性や副作用も確認されていません。唯一アルロースにより下痢が起こることがあります。これは難消化性糖類に共通した作用です。アルロースでは体重1kgあたり 0.55g (男性0.5g、女性0.6g)までは下痢が起こらないとされています。ただし個人差がありますので、敏感な方はこれ以下でも下痢が起こることがあります。また、ヒト試験での報告を読みますと、嘔気や腹痛など消化器系の症状が出ることがありますが、アルロースの対象として用いられた糖質と比べて明らかに高い頻度で発現しているものではありません。
アルロースを用いた機能性表示食品
機能性表示食品とは、事業者の責任において、科学的根拠に基づいた機能性を表示した食品です。 販売前に安全性及び機能性の根拠に関する情報などが消費者庁長官へ届け出られたものです。ただし、特定保健用食品とは異なり、消費者庁長官の個別の許可を受けたものではありません。機能性表示食品は医薬品ではありませんから、疾病の診断、治療、予防を目的としたものではありません。疾病のある方、薬を服用されている方は、医師、薬剤師に ご相談くださることをお勧めします。
消費者庁「機能性表示食品」って何?
(https://www.caa.go.jp/notice/assets/150810_1.pdf)
機能性表示食品の表示があるアルロースの場合には、 一日に摂取する量の目安や 摂取方法使い方が示されていますので、 それを参考にしてください。
アルロースを用いた一般製品(機能性表示食品でないもの)
特定の機能を期待するものではありませんので、摂取量などに特に制限はないことになります。摂取量が多ければ多いほど効果が高いというものではありません。これまでの研究やヒト試験では、1 回 5g 程度で血糖上昇抑制作用や脂肪燃焼促進作用などがみられていることから、使用の目安量になると考えられます。アルロースの量として1 日5g で始めるのがお勧めです。糖尿病や高脂血症などで医療機関を受診され治療をされている方については、始められるにあたり主治医にご相談されることをお勧めします。
希少糖含有シロップ
アルロースなどの希少糖が含有されたシロップは、健康や体重を気にされている方が生活習慣病の予防として(病気にならないための対策として)活用することが望ましく、普段の食生活で砂糖に置き換えて希少糖含有シロップを使用することをお勧めします。 このように、病気になる前の方が食品として希少糖を摂取し、病気になる可能性を低減し、健康寿命を延ばすことに貢献できると期待しています。ただし、シロップにはブドウ糖や果糖も含まれるため、既に糖尿病などを発症している方は、医師に相談するなど慎重に使ってください。
アルロースの植物分野への応用
希少糖が作用するのは動物だけではありません。植物に対しても大きな影響を与えることが分かってきました。
香川大学農学部では、いくつかの希少糖がイネなどの病害虫防御関連遺伝子の発現を誘導することや、植物の生長を調節する作用を持つことを発見し、耐病性誘導や生育調節用の資材開発や利用法などの研究も進めています。
実用化に向けては、現在香川大学と民間企業の連携で農業資材開発が進められています。この農業資材開発ですが自然界に存在する天然物で、食べられる物質である糖を使うため人にも環境にも優しく、安全性という視点で今までにない農薬等の開発につながると期待されています。


発芽して数日経ったイネ。僅かにアルロースを含んだ水溶液を与えると、生長が抑制されます。


アルロース水溶液を与えた部分の生長が抑制され、文字や絵を簡単に浮き出させることも可能です。ズイナはアルロースを自身で生産・蓄積するとても珍しい植物です。その理由は明らかにはなっていませんが、ズイナは、アルロースが含まれた葉を落とし、周囲に生える他の植物の成長を阻害して、自らに優位な生育環境を作ってきたと考えられています。自然淘汰された希少糖を自ら生産・蓄積する“植物のシーラカンス”ズイナは、特殊な方法で生存競争を戦ってきたと推測されます。
学名 Itea japonica Oliver 科名 ズイナ Iteaceae
日本固有の落葉低木。幹は高さ1-2m、分枝する。葉は互生し、卵状楕円形から卵形、先は尖り、鋸歯がある。花期は5-6月。花序は総状で長さ5-17cm、枝に頂生する。花弁は5枚、狭披針形、長さ3-5mmで白色。蒴果は広卵形。種子は長さ約8mmで黒熟し、網模様が見られる。 本州(近畿地方南部)・四国・九州に分布。(出典:筑波実験植物園(つくば植物園)ウェブサイト)



世界の糖の動向とシュガーラベリング


砂糖の摂取量を減らすべき!という世界的潮流
糖(シュガー)といえば、砂糖に代表される甘さが魅力です。しかし、糖がもたらす弊害として糖尿病患者の増加が世界的に深刻になってきています。国際糖尿病連合(IDF)の発行した「糖尿病アトラス第9版」によると、糖尿病有病者数は2019年に4億6,300万人であり、2040年までに7億人に増加すると予測されています。日本でも、厚生労働省「2019年国民健康・栄養調査結果」の推計で、男性の19.7%、女性の10.8%が「糖尿病が強く疑われる」と判定されました。
そのような動向を受けて、世界保健機構(WHO)は2015年3月に、成人及び児童の1日当たり遊離糖類摂取量をエネルギー総摂取量の10%未満に減らすよう推奨し、また5%まで減らすなら、更に健康効果は増大するという新指針を発表しました。日本人の場合、1日に約2000キロカロリーを摂取しているので、5%は100キロカロリーになり、1グラム4キロカロリーの砂糖では25gに相当します。一般的に炭酸飲料1本には30~40gの砂糖が含まれており、それだけで1日分を超えてしまいます。
砂糖の摂取量を減らすために、甘味度の高い人工甘味料の開発が進みました。上手に摂取することにより甘味を楽しみながらカロリー摂取を押さえるために使われています。また、2023 年 5 月に世界保健機関(WHO)は、体重管理や非感染性疾患(NCD=生活習慣病と同
義)のリスク軽減を目的として「非糖類甘味料」を長期使用しても効果がなく、むしろ健康リスクを
引き起こす可能性があることを警告しました。非糖類甘味料にはサッカリン、アスパルテーム、アセ
スルファム K などの人工甘味料やステビア、グリチルリチンなどの天然甘味料が含まれます。一方
アルロースは低カロリー糖類に分類され非糖類甘味料ではありません。
シュガーラベリング
希少糖は「糖」です。アルロースは化学構造的には「糖」の構造を持ちますが、栄養学的にはこれまでの「糖」と異なる性質を持っています。
アメリカのCCC(Calorie Control Council)は世界を代表する食品企業で構成された団体です。この団体では、アルロースの表記について活発に議論がおこなわれています。食品や飲料にゼロカロリー甘味料のみを使えば「無糖」や「糖類ゼロ」と表記されるのですが、アルロースはカロリーゼロではあるもののあくまで「糖」であり「無糖」というカテゴリーに属さないのではという意見がありました。そこで2023年開催の第8回国際希少糖学会で、北米、欧州、アジアからそれぞれを代表する企業が参加しシュガーラベリングについて議論を行い、「化学的構造から糖であるものの、ブドウ糖・砂糖とは異なるカテゴリーにするべきであること」を学会の統一意見として表明することを決めました。表記方法は今回の統一意見を各国に持ち帰り、それぞれの規制に合わせて審議するという方向で進んでいます。
世界に広がるアルロース
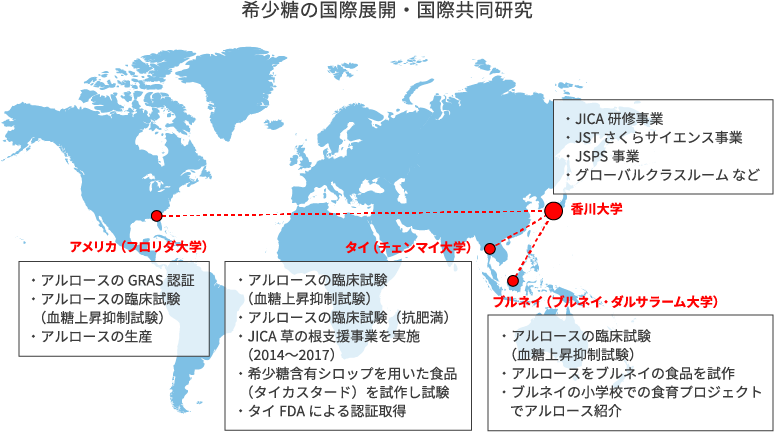
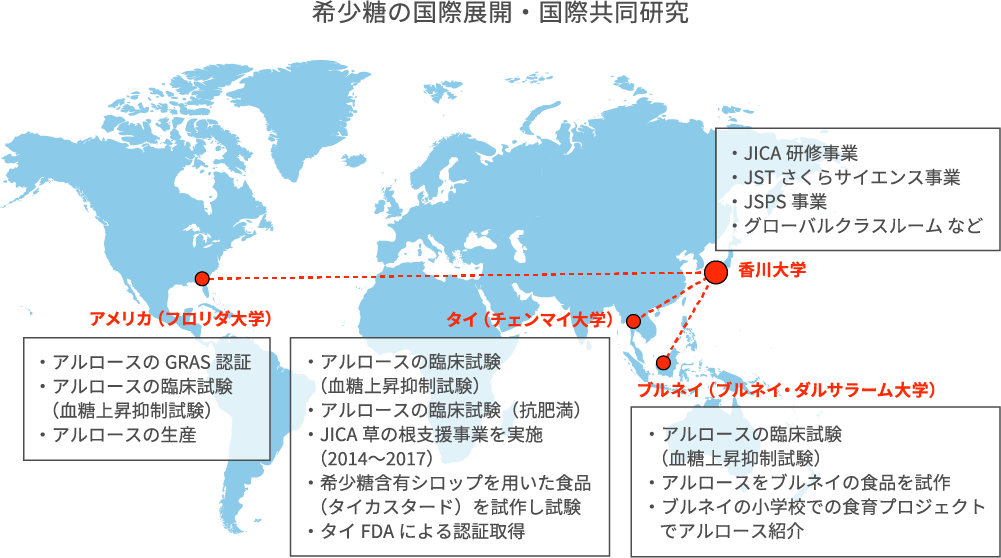
アルロースの研究はアメリカやアジア各国で進んでいます。 タイのチェンマイ大学と香川大学は共同研究を展開しており、アルロースの血糖値上昇抑制作用・抗肥満作用の臨床試験、カスタードやタイ茶に希少糖含有シロップを使用する取り組みを始めています。また肥満の多い国でありアルロースへの期待が高いブルネイでも臨床試験を進めています。アルロースを用いた食育事業も展開しています。そしてアメリカ・フロリダでも血糖値上昇抑制試験の臨床試験を行いました。これらすべての試験で、アルロースには血糖値上昇抑制効果があることが示されました。
(J Nutr Sci Vitaminol(Tokyo). 2024; 70(3): 203-209, BMJ Open Diabetes Res Care. 2021; 9(1): e001939)
イスラム教徒が行うラマダンの断食中、イフタール (日没時の断食休憩) の食事後に食後高血糖がよく見られます。そこで香川大学内分泌代謝チームは、アルロースが 2 型糖尿病患者の食後高血糖を改善するかどうかを、10 日間連続する前向き単群研究デザインで実施し、アルロース8.5gをイフタール前に摂取することで、食後高血糖を改善する可能性を指摘しました。(Diabetol Metab Syndr. 2022;14(1):86)
世界では、10カ国以上で既にアルロースが販売されています。そして多くの食品や飲料に用いられており、製品数は近年急速に増えています。特にアメリカでは安全な食品として米国食品医薬品局(FDA) より安全性(GRAS認定)が早くから確認されました。
2019年にFDAは、希少糖アルロースは米国栄養表示における糖類(Total Sugars)分類から除外するという指針を発表しました。アメリカではアルロースを使用しても、糖類ゼロ、添加糖ゼロ、カロリーゼロとして扱うことが可能となっています。韓国でも同様の認可がなされました。残念ながら日本では未だ認められていません。アメリカや韓国では、アルロースがどんどん使われるようになっています。
